คำจำกัดความของไอออนบวกหรือลบ

อย่างที่เราทราบกันดีอยู่แล้วว่า อะตอม พวกมันถูกสร้างขึ้นโดย อนุภาค. ในอนุภาคย่อยทั้งสามประเภท มีเพียงนิวตรอนเท่านั้นที่ไม่มีประจุไฟฟ้า โปรตอนมีประจุไฟฟ้าเป็นบวกแทนในขณะที่อิเล็กตรอนมีประจุลบ เฉพาะอิเล็กตรอนซึ่งครอบครองรอบนอกของอะตอมเท่านั้นที่สามารถถ่ายโอนจากอะตอมหนึ่งไปยังอีกอะตอมหนึ่งได้ในขณะที่โปรตอนในนิวเคลียสรักษาจำนวนให้คงที่ ในบทเรียนนี้จากครู เราจะมาดูกันว่าจะเกิดอะไรขึ้นเมื่ออะตอมหรือโมเลกุลได้รับหรือสูญเสียอิเล็กตรอน คือเราจะเห็น ความหมายและตัวอย่างของไอออนบวกหรือลบ
ดัชนี
- ไอออนคืออะไร? นิยามง่ายๆ
- การก่อตัวของไอออน: สัมพรรคภาพทางไฟฟ้าและอิเล็กโตรเนกาติวีตี้
- ไอออนลบคืออะไร? พร้อมตัวอย่าง
- ไอออนบวกคืออะไร? พร้อมตัวอย่าง
ไอออนคืออะไร? คำจำกัดความง่าย
อา ไอออน เป็นอะไรก็ได้ อะตอมหรือโมเลกุลที่มีประจุไฟฟ้าสุทธิ. กล่าวคือเป็นอะตอมหรือชุดของอะตอมที่เชื่อมต่อกันซึ่งมีประจุไฟฟ้า ไม่ได้รับการชดเชย. การสลายตัวของประจุนี้เกิดขึ้นเมื่ออิเล็กตรอนตั้งแต่หนึ่งตัวขึ้นไปเข้าร่วมหรือออกจากอะตอมหรือชุดของอะตอม
ไอออนเป็นดังนี้ อะตอมหรือโมเลกุลที่มีประจุ เนื่องจากการได้รับหรือสูญเสียของอิเล็กตรอน (อนุภาคของอะตอมที่มีประจุลบและมวลเล็กน้อย)
ประเภทไอออน: monatomic และ polyatomic
หากเราพิจารณาถึงองค์ประกอบของไอออน จะแบ่งออกเป็นสองประเภท: โมโนอะตอมมิกไอออนและโพลิอะตอมมิกไอออน
- ตามชื่อที่แนะนำ โมโนอะตอมมิกไอออน ที่เกิดจาก อะตอมเดียว.
- สารประกอบไอออนิก o ไอออน polyatomic คืออะตอมที่พันธะโควาเลนต์ (ใช้อิเล็กตรอนร่วมกันตั้งแต่หนึ่งคู่ขึ้นไปในพันธะ) มีจำนวน นิวตรอน ในโมเลกุลที่แตกต่างจากจำนวนอิเล็กตรอนทั้งหมด
- ไอออน polyatomic มักจะมี ออกซิเจน และพวกมันมักจะมีโครงสร้างที่มีอะตอมตรงกลางซึ่งองค์ประกอบที่เหลือที่ประกอบเป็นโมเลกุลจะถูกจัดเรียง
- ประจุของโมโนอะตอมมิกไอออน ขององค์ประกอบที่เป็นตัวแทน (ตระกูลที่ 1 และ 2 ของตารางและตระกูลที่ 13 ถึง 17 ของตารางธาตุ) สามารถอนุมานได้อย่างง่ายดายหากทราบตำแหน่งภายในตารางธาตุ ในกรณีเหล่านี้ อะตอมจะได้รับหรือสูญเสียอิเล็กตรอนเพื่อที่จะไปถึงการกำหนดค่าของก๊าซมีตระกูลในช่วงเวลาของมัน (ส2พี6) หรืออะไรที่เหมือนกันให้เติมเต็ม กฎออกเตต.
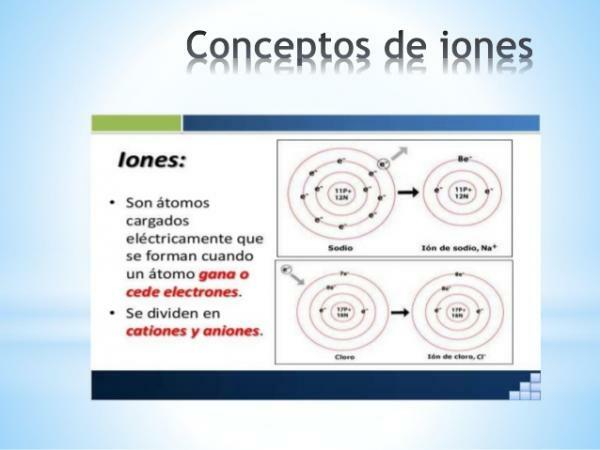
ภาพ: Slideshare
การก่อตัวของไอออน: อิเล็กโตรฟฟินิตี้และอิเล็กโตรเนกาติวีตี้
ความสามารถของอะตอมหรือโมเลกุลต่อ ฟอร์มไอออน ถูกกำหนดโดยคุณสมบัติเป็นระยะสองประการ: อิเล็กโตรฟฟินิตีและอิเล็กโตรเนกาติวีตี้. คุณสมบัติทั้งสองเพิ่มมูลค่าในช่วงเวลาหนึ่งและลดลงเมื่อเราลงมาจากกลุ่มหรือตระกูลของตารางธาตุ
ความสัมพันธ์ทางไฟฟ้าaffเรียกอีกอย่างว่าความสัมพันธ์ระหว่างอิเล็กตรอนเป็นสมบัติของอะตอมที่กำหนดให้เป็นความสามารถของอะตอมในการดึงดูดอิเล็กตรอน ในกรณีของสารประกอบมีคุณสมบัติคล้ายคลึงกันเรียกว่า อิเล็กโตรเนกาติวีตี้ ซึ่งถูกกำหนดให้เป็นความสามารถของอะตอมในการดึงดูดอิเล็กตรอนเมื่อมันสร้างพันธะกับอะตอมอื่น คุณสมบัติทั้งสองจึงกำหนดแนวโน้มขององค์ประกอบที่จะจับหรือสูญเสียอิเล็กตรอน
พันธะไอออนิก
ในรูปของแข็ง ไอออนจะก่อตัวเป็นสารประกอบหรือ ผลึกไอออนิก (เกลือ) ที่เกิดจากการรวมตัวของอิออนของเครื่องหมายต่าง ๆ เข้าด้วยกันโดยวิธี พันธะไอออนิก. ตัวอย่างที่รู้จักกันดีที่สุดของสารประกอบประเภทนี้คือเกลือทั่วไป (โซเดียมคลอไรด์: NaCl)
พันธะไอออนิกประกอบด้วยการรวมตัวของไอออนที่มีเครื่องหมายต่างกันโดยใช้แรงดึงดูดจากไฟฟ้าสถิต (แรงดึงดูดระหว่างประจุของเครื่องหมายตรงข้าม) องค์ประกอบที่มีอิเล็กโตรเนกาติวีตีหรือความสัมพันธ์ทางไฟฟ้าแตกต่างกันมาก (ธาตุโลหะและอโลหะ) แทรกแซงในลิงก์ประเภทนี้ ในกรณีส่วนใหญ่ สารประกอบไอออนิกเหล่านี้คือ ละลายในน้ำ และตัวทำละลายขั้วอื่นๆ
ในสารละลายที่เป็นน้ำ สารประกอบไอออนิกจะแยกตัวเป็นไอออนอิสระ ซึ่งเรียกว่า อิเล็กโทรไลต์เนื่องจากการมีอยู่ของมันในสารละลายทำให้น้ำทำหน้าที่เป็นตัวนำไฟฟ้า
ไอออนลบคืออะไร? พร้อมตัวอย่าง.
ไอออนลบ พวกเขาถูกเรียกว่า แอนไอออน. ในทุกกรณี พวกมันคืออะตอมขององค์ประกอบหรือโมเลกุลที่ไม่ใช่โลหะที่มีองค์ประกอบที่ไม่ใช่โลหะ องค์ประกอบเหล่านี้มีลักษณะเฉพาะโดยมีสัมพรรคภาพทางไฟฟ้าและอิเล็กโตรเนกาติวีตี้สูงมาก นั่นคือพวกมันคือไอออนที่เกิดจากองค์ประกอบที่มี มีแนวโน้มสูงที่จะจับอิเล็กตรอน.
แอนไอออนโมโนโมโน: ความหมายและตัวอย่าง
พวกมันคือแอนไอออนที่เกิดจากอะตอมของธาตุที่ไม่ใช่โลหะ (กลุ่มที่ 13 ถึง 17 ของตารางธาตุ) ซึ่งได้รับอิเล็กตรอนตั้งแต่หนึ่งตัวขึ้นไป แอนไอออนเหล่านี้มีโครงสร้างอิเล็กทรอนิกส์ก๊าซมีตระกูลเหมือนกัน (s2พี6) ในเปลือกอิเล็กตรอนชั้นนอกสุด (วาเลนซ์เชลล์)
ตัวอย่าง:
- คลอไรด์ไอออน: Cl-
- ฟลูออไรด์ไอออน: F-
- ไอออนไอโอไดด์: I-
- ซัลไฟด์ไอออน: S-2
- ไนไตรด์ไอออน: N-3
แอนไอออน Polyatomic: ความหมายและตัวอย่าง
พวกมันเป็นไอออนที่มีประจุลบซึ่งเกิดขึ้นจากอะตอมของธาตุอโลหะตั้งแต่สองอะตอมขึ้นไปที่เชื่อมโยงกันด้วยพันธะโควาเลนต์ พวกเขาเป็นไอออน polyatomic ที่พบบ่อยที่สุด แอนไอออน polyatomic ที่พบมากที่สุดคือ oxoanion ซึ่งประกอบด้วยอะตอมกลางที่ไม่ใช่โลหะและมีออกซิเจน
โดยทั่วไปจะถือว่าเป็นสารประกอบทางเคมีที่ได้จากสารประกอบที่เป็นกรดสูญเสียโปรตอนหนึ่งตัวหรือมากกว่า (H+). แอนไอออน polyatomic เหล่านี้สามารถเก็บไฮโดรเจนบางส่วนไว้ในโครงสร้าง ซึ่งทำให้มีลักษณะกรดบางอย่าง (ความสามารถในการให้โปรตอน)
ตัวอย่าง:
- ไนเตรตไอออน: NO3-
- เปอร์แมงกาเนตไอออน: MnO4-
- ฟอสเฟตไอออน: PO4-3
- ไฮโดรเจนคาร์บอเนตหรือไอออนไบคาร์บอเนต: HCO3-
- ไอออนซัลไฟต์: SO3-2
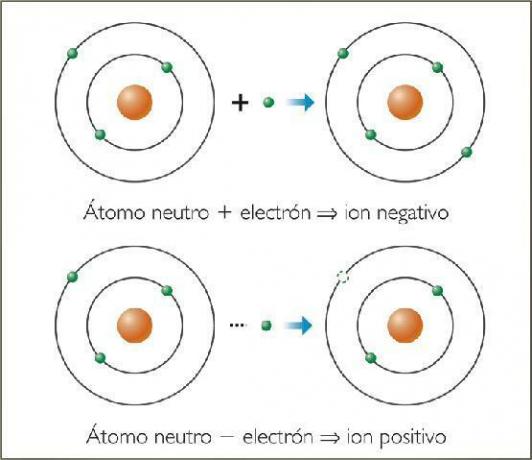
ภาพ: ธรรมชาติบำบัด
ไอออนบวกคืออะไร? พร้อมตัวอย่าง.
ไอออนบวกเรียกว่า คation. ในเกือบทุกกรณี พวกมันคืออะตอมของธาตุโลหะหรือโมเลกุลที่มีธาตุโลหะ องค์ประกอบเหล่านี้มีลักษณะเฉพาะโดยมีสัมพรรคภาพทางไฟฟ้าและอิเล็กโตรเนกาติวีตี้ต่ำมาก ซึ่งเป็นสาเหตุที่ทำให้มีแนวโน้มที่ชัดเจนที่จะสูญเสียอิเล็กตรอน
Monatomic cations: ความหมายและตัวอย่าง
พวกมันคือไอออนที่มีประจุบวก (เนื่องจากการสูญเสียอิเล็กตรอน) ที่เกิดจากอะตอมเดี่ยวของธาตุโลหะ ในกรณีนี้ ไอออนบวกเกิดขึ้นจากการสูญเสียอิเล็กตรอนที่ยอมให้ธาตุล้างชั้นอิเล็กทรอนิคส์ที่อยู่นอกสุดและได้รับการกำหนดค่าของก๊าซมีตระกูล2พี6) จากระดับล่าง เป็นไอออนบวกชนิดที่พบบ่อยที่สุด
ตัวอย่าง:
- ไฮโดรเจนหรือไฮโดรเจนไอออน (เรียกอีกอย่างว่าโปรตอน): H+
- โซเดียมไอออนบวก: Na+
- ไอออนบวก (III) หรือไอออนบวกของเฟอริก: Fe+3
- แคลเซียมไอออนบวก: Ca+2
- ทองแดง (II) หรือคิวปริกไอออน: Cu+2
Polyatomic cations: ความหมายและตัวอย่าง
Polyatomic cations เกิดจากอะตอมตั้งแต่สองอะตอมขึ้นไป พวกมันหายาก ที่อุดมสมบูรณ์ที่สุดคือที่เรียกว่าไพเพอร์ homopolyatomic ซึ่งมีมากกว่าหนึ่ง อะตอมของธาตุเดียวกัน ในกรณีของไอออนไตรไฮโดรเจน เป็นโมเลกุลที่มีมากที่สุดแห่งหนึ่งใน จักรวาล. Polyatomic cations ที่เกิดจากอะตอมของธาตุต่าง ๆ นั้นไม่ธรรมดา แต่มีลักษณะเฉพาะโดย การปรากฏตัวของไฮโดรเจนและถือว่าเกิดขึ้นเมื่อสารประกอบพื้นฐานจับโปรตอน (ฮ+).
ตัวอย่าง:
- แอมโมเนียมไอออนบวก: NH4+
- ออกโซเนียมไอออนบวก: HO3+
- ฟอสโฟเนียมไอออนบวก: PH3+
- ไตรไฮโดรเจนไอออนบวกหรือไฮโดรเจนโมเลกุลที่โปรตอน: H3+
- Dimercury ไอออนบวก: Hg2+2
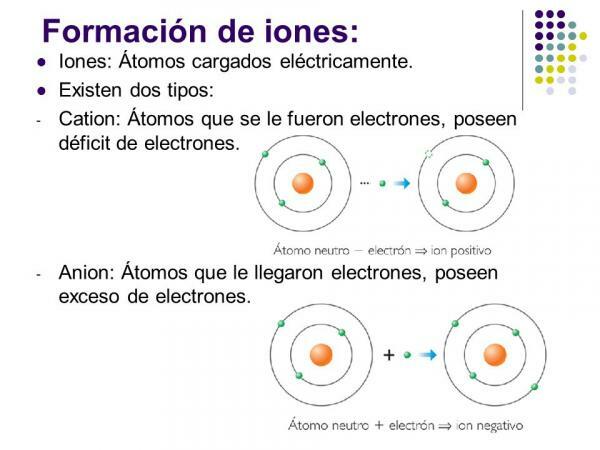
ภาพ: ดาวเคราะห์
หากคุณต้องการอ่านบทความเพิ่มเติมที่คล้ายกับ ไอออนลบและประจุบวก: ความหมายและตัวอย่างเราขอแนะนำให้คุณป้อนหมวดหมู่ของเรา อะตอม.
บรรณานุกรม
Alejandrina Gallego Picó, Rosa Mª Garcinuño Martínez, Mª José Morcillo Ortega, Miguel Ángel Vázquez Segura (2018) เคมีพื้นฐาน. มาดริด: Uned