10 -те вида химични елементи (обяснени и класифицирани)
Колко химични елемента трябва да съществуват във Вселената? Този въпрос все още има дълъг път, тъй като учените от време на време създават свои собствени изкуствени химични елементи.
Това, на което обаче можем да отговорим, е колко вида химични елементи трябва да съществуват, нещо, което ще разберем по -нататък.
- Свързана статия: "11 -те вида химични реакции"
Видовете химични елементи
В природата можем да намерим всякакви вещества. Тези вещества обикновено не се намират в чисто състояние, а са резултат от комбинацията от различни елементи или материали, които чрез различни реакции, процеси и периоди от време са породили всички видове материя. Няма нищо във Вселената, което да не е резултат от комбинацията от атоми, принадлежащи към различни видове химични елементи, което ще видим в дълбочина.
Въпреки това, преди да разгледаме видовете химични елементи, нека направим малък преглед на науката в гимназията и си спомнете какви са химическите елементи.
Ние наричаме "химичен елемент" материя, която е съставена от същия тип атом, тоест вещество, което е атомно чисто.
Химическите елементи не могат да се разлагат на по -прости и се класифицират в периодичната таблица на елементите като чисти материали на Вселената.Но внимавайте! Не трябва да бъркаме елементите с прости вещества, тъй като в определени случаи могат да се състоят два или повече атома от един и същ елемент молекули, групирани по различни начини, които причиняват промяна в някои физични свойства на въпросния елемент, като тези случаи са изотопи. Например диамантът и въглеродът са вещества, направени от химичния елемент въглерод (С). но това е организирано по различни начини и води до два напълно различни материала.
Карл Сейгън Каза, че ние сме звезден прах, отразяващ звездите. Тази красива фраза не е просто метафора, а научен факт. Химическите елементи се образуват, доколкото ни е известно, вътре в звездите са резултат от комплекс процеси на синтез и атомно делене, които генерират все по -тежки елементи, резултат от процес, наречен нуклеосинтеза.
Повечето от известните елементи могат да бъдат получени от природата, открити спонтанно или образуващи съединения с други елементи като уран (U), въглерод (С), силиций (Si), сребро (Ag) или злато (Au). Други, от друга страна, са произведени в лаборатории като америций (Am), беркелий (Bk) или курий (Cm). Какъвто и да е методът му за получаване или ако той присъства в природата, в зависимост от неговите свойства, въпросният химичен елемент ще има някои или други приложения.
Понастоящем са известни около 118 химични елемента, въпреки че като се има предвид, че хората са успели да произвеждат нови елементи, е въпрос на време периодичната таблица да се разшири.
- Може да се интересувате от: „Двата вида електричество (обяснено)“
Основните видове химични елементи
Основните видове химични елементи са представени в периодичната таблица, система от класификация, създадена от руския химик Дмитрий Менделеев (1834-1907), който полага основите си през 1869. Химическите елементи са подредени визуално въз основа на техните свойства и характеристики.
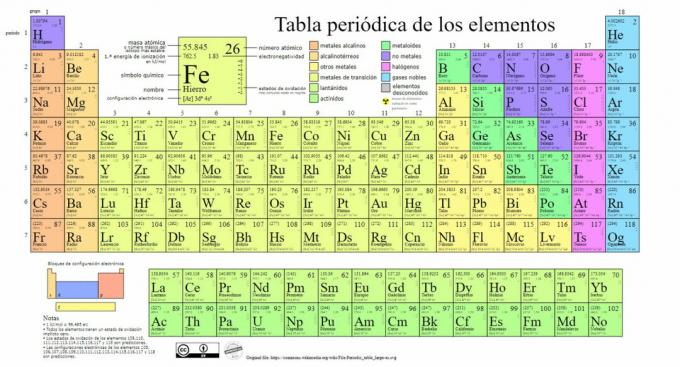
С течение на времето и тъй като химията направи важни научни открития, тази таблица ще се разширява последователно, достигайки до сегашната си форма със 118 -те известни досега елемента.
Понастоящем в тази таблица можем да намерим следните видове химични елементи:
1. Метали
Металите са химични елементи, които обикновено съдържат между един и три електрона в последната орбита на своя атом, електрони, които могат лесно да се прехвърлят превръщайки ги в проводници на топлина и електричество.
Металите обикновено са пластични и пластични, с характерен блясък, чиято интензивност зависи от движението на електроните, съставляващи техните атоми. През повечето време металите са твърди при стайна температура, с изключение на живака.
Сред металите откриваме злато (Au), сребро (Ag), мед (Cu) и алуминий (Al), чиито физически характеристики ги правят великолепни проводници на електричество, въпреки че присъствието им в природата е много разнообразно, отразено в разликата между теглото им.
Смята се, че 75% от съществуващите в природата химични елементи са метали, докато останалите 25% ще бъдат съставени от благородни газове, металоиди и други видове.
В тази категория има класификации, които откриват актиниди, лантаниди, преходни метали, алкални метали, алкалоземни метали и други метали.
- Свързана статия: „10 храни с високо съдържание на цинк“
1.1. Лантаниди
Елементите на лантанидите се намират в находища, съставени от много минерали. Те са бели метали, които лесно се окисляват при контакт с въздуха. Сред тях откриваме лантан (La), прометий (Pm), европий (Eu) и итербий (Yb).

- Може да се интересувате от: "5 -те вида химически връзки: така е съставена материята"
1.2. Актиниди
Всички изотопи на актинидите са радиоактивни. Сред тях откриваме актиний (Ac), уран (U), плутоний (Pu) и айнщайний (Es).
1.3. Преходни метали
Преходните метали се намират в централната част на периодичната система. Основната му характеристика е, че имат електронна конфигурация на "d" орбиталата, частично изпълнена с електрони.
В тази група има вещества от всякакъв вид и според най -широката й класификация, тя би съответствала на химични елементи от 21 до 30, от 39 до 48, от 71 до 80 и от 103 до 112, като общо са четиридесет и сред тях ще открием ванадий (V), рутений (Ru), сребро (Ag), тантал (Ta) и лауренсио (Lr).

1.4. Алкални метали
Алкалните метали са група от шест елемента, съставени от литий (Li), натрий (Na), калий (К), рубидий (Rb), цезий (Cs) и франций (Fr). Те са лъскави, меки метали, силно реактивни при нормална температура и налягане и лесно губят външния си електрон, разположен в тяхната "s" орбитала.
1.5. Алкални земи
Алкалоземните метали са група елементи, в които откриваме берилий (Be), магнезий (Mg), калций (Ca), стронций (Sr), барий (Ba) и радий (Ra). Името му идва от името, дадено на неговите оксиди, "земя", които имат основни или алкални свойства.
Алкални земи те са по -твърди от алкални, блестят и са добри електрически проводници. Те са по -малко реактивни от алкалните и действат като добри редуциращи агенти. Те имат способността да образуват йонни съединения и всички те имат по два електрона в най -външната си обвивка.

1.6. Други метали
Категорията "други метали" е вид вещества, които се срещат тук, защото всъщност не знаете къде да ги поставите.
Те са метални елементи, разположени в периодичната таблица заедно с металоидите, в рамките на p блока. Те са склонни да бъдат меки с ниски точки на топене. Сред тях са алуминий (Al), индий (In), калай (Sn) и бисмут (Bi) и други.

2. Без метали
Неметалите обикновено притежават между пет и седем електрона в последната си орбита, свойство, което прави че те печелят електрони, вместо да се откажат от тях и по този начин успяват да имат осем електрона, които по този начин ги стабилизират като атоми.
Тези елементи те са много лоши проводници на топлина и електричество. В допълнение към това, те нямат характерен блясък, не са много пластични, не са много пластични и са много крехки в твърдо състояние. Те не могат да се търкалят или опъват, за разлика от металите.
Те са от съществено значение за биологичните системи, тъй като присъстват в органични съединения, като сяра (S), въглерод (С), кислород (О), водород (Н) и йод (I).

- Свързана статия: „20 -те вида скъпоценни камъни (описани и със снимки)“
3. Металоиди
Както подсказва името им, металоидите са междинна класификация между метали и неметали, които имат свойства и на двете групи. Това се дължи на факта, че те имат четири атома в последната си орбита, междинно количество спрямо това на металите и неметалите.
Тези химически елементи провеждат електричество само в една посока, като не позволяват то да се извършва в обратна посока, както в металите. Пример за това се намира в силиций (Si), металоид, използван при производството на полупроводникови елементи за електронната промишленост благодарение на това свойство.
Други металоиди са: бор (В), арсен (As), антимон (Sb) и полоний (Po).

4. Халогени
Халогените са група от шест елемента, които те са склонни да образуват молекули, съставени от два атома (двуатомни), които са много химически активни поради тяхната електроотрицателност.
Тези вещества обикновено се появяват под формата на йони, тоест електрически заредени молекули, които в този случай са моноотрицателни, силно окисляващи. Това означава, че халогените са разяждащи и корозивни вещества.
Халогените са: флуор (F), хлор (Cl), бром (Br), йод (I), астат (At) и тенез (Ts).

5. Благородни газове
Благородните газове са група от седем, чието естествено състояние е газообразно. Те обикновено се появяват под формата на двуатомни молекули с много ниска реактивност, тоест не реагират с други елементи, съставляващи други вещества и поради същата причина те са известни като инертни газове. Това е така, защото в последната му орбита има възможно най -голям брой електрони за това ниво, общо осем.
Тази избрана група от елементи се състои от хелий (He), неон (Ne), аргон (Ar), криптон (Kr), ксенон (Xe), радон (Rn) и оганезон (Og), известен преди като унонокций.


