Para que serve a TABELA PERIÓDICA?
A tabela periódica é um sistema de classificação de elementos atômicos inventado em 1869 pelo químico russo Dmitri Mendeleev e posteriormente reorganizado e atualizado por outros químicos até chegar a sua aparência atual. Apesar de ser uma ferramenta que tem se mostrado útil ao longo da história (por isso continua a ser usada e atualizada), é uma Tão entediante de aprender e entender, é por isso que todos nós nos perguntamos "Para que serve a mesa? periódico? ".
Se você quer saber para que serve a tabela periódica e por que é importante entender suas propriedades, continue lendo esta lição de um PROFESSOR.
Índice
- Classificação da tabela periódica
- Encontrar o nome ou símbolo de um elemento com a tabela periódica
- Conheça a massa atômica de um elemento
- Conheça o número atômico de um elemento
- Preveja o raio atômico de um elemento
- Compare a energia de ionização de dois elementos
- Encontrando a eletronegatividade de um elemento químico
- Compare a afinidade eletrônica de dois elementos
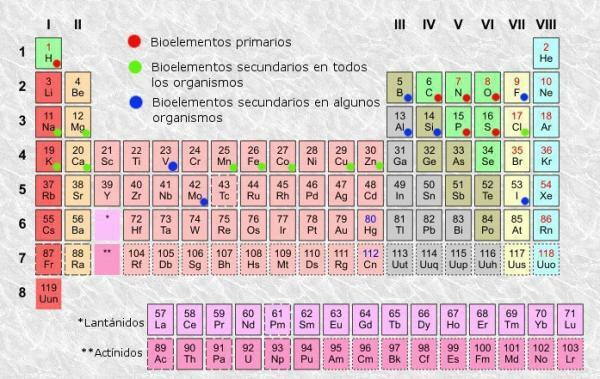
Classificação da tabela periódica.
Como em qualquer mesa, em a tabela periódica dos elementos, podemos distinguir colunas (verticais) e linhas (horizontais). Na tabela periódica, existem 18 colunas ou grupos e 7 linhas ou períodos.
Além disso, você poderá verificar que, normalmente, em cada uma das caixas da tabela, aparecem pelo menos as seguintes informações:
- Símbolo do elemento químico: abreviaturas ou sinais que são usados para identificar os elementos. Eles geralmente consistem em uma ou duas letras, das quais a primeira é sempre maiúscula.
- Nome do elemento químico: nome do elemento químico que corresponde à abreviatura superior. Geralmente está abaixo do símbolo.
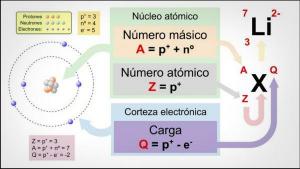
- Número atômico: número total de prótons que cada átomo desse elemento possui. Geralmente aparece no canto superior esquerdo da caixa do item (ou no canto superior direito de tabelas mais completas).
- Massa atômica: a massa de um átomo pode normalmente ser considerada como a massa total de prótons e nêutrons em um único átomo. Está disponível abaixo do nome do elemento nas tabelas mais simples, embora em outras possa aparecer na parte superior direita da caixa do elemento.
Existem tabelas periódicas que incluem outras informações mais complexas e específicas, como estados de oxidação (útil ao formular compostos químicos, por exemplo), energia de ionização, eletronegatividade, etc., mas tabelas periódicas básicas geralmente fornecem informações suficientes e geralmente são suficientes para o usuário médio, que a partir dela pode encontrar informações como a que apresentamos a seguir.

Descubra o nome ou símbolo de um elemento com a tabela periódica.
Às vezes sabemos o símbolo do elemento químico mas não sabemos seu nome. Em outras ocasiões, sabemos o nome do elemento químico, mas não sua abreviatura ou símbolo. Na verdade, é muito fácil que isso tenha acontecido com você na aula.
Nestes casos, podemos utilizar uma tabela periódica, sem a necessidade que seja complexa, e consultar os dados que faltam com rapidez e precisão.
Conheça a massa atômica de um elemento.
Às vezes, sabemos o elemento químico com o qual estamos lidando, mas precisamos saber seu massa atômica, isto é, quanto pesa um átomo desse elemento.
Essas informações serão úteis, por exemplo, ao realizar as seguintes tarefas:
- Calcule a quantidade específica de uma substância.
- Analise os resultados obtidos nos testes ou experimentos.
- Calcule a porcentagem da massa.
- Compreenda as massas molares precisas de moléculas complexas.
Conheça o número atômico de um elemento.
O número atômico é número total de prótons que um átomo de um elemento possui. Em um átomo eletricamente neutro, diferente de um cátion (carregado positivamente, com um elétron a menos que seu estado normal) ou um ânion (carregado negativamente, com um elétron a mais do que seu estado normal), o número de prótons é igual ao de elétrons.
O número de prótons é o fator decisivo na hora de distinguir um elemento do outro, já que o número de elétrons ou nêutrons não altera o tipo de elemento.

Preveja o raio atômico de um elemento.
O raio atômico é a metade da distância entre o centro de dois átomos do mesmo elemento que mal se tocam. Neste caso, conheça o posição de um elemento químico na tabela periódica Pode nos ajudar a descobrir seu raio atômico aproximado ou comparado a outro elemento. Para isso, temos que saber que o raio atômico:
- Ele aumenta à medida que avançamos do início para o fim da tabela periódica.
- Ele desce à medida que avançamos da esquerda para a direita na tabela periódica.
Dessa forma, o cálcio é menor do que o rubídio, mas maior do que o ferro.
Aprender mais sobre Qual é o raio atômico com esta outra vídeo-aula de um PROFESSOR.
Compare a energia de ionização de dois elementos.
O energia de ionização é o energia necessária para remover um elétron do átomo de um elemento. Nesse caso, se soubermos a posição de dois elementos na tabela periódica, podemos saber de qual elemento será mais fácil "tirar" um elétron. Teremos apenas que levar em consideração que:
- A energia de ionização diminui à medida que sobe e desce na tabela periódica.
- A energia de ionização aumenta à medida que você se move da esquerda para a direita da tabela periódica.
Entre o berílio e o oxigênio, o oxigênio tem mais energia de ionização. Se compararmos oxigênio e enxofre, que está no mesmo grupo, mas no próximo período, o oxigênio também tem maior energia de ionização, pois é maior na tabela periódica.
Descubra a eletronegatividade de um elemento químico.
Eletro-negatividade é o capacidade de um átomo de atrair elétrons. Na prática, isso se traduz na capacidade de formar uma ligação química. Para saber se um elemento químico terá grande capacidade de formar uma ligação química ou não, basta levar em consideração o padrão que segue na tabela periódica, ou seja:
- Ele desce à medida que sobe e desce.
- Ele aumenta à medida que você se move da esquerda para a direita.
Como no caso anterior, o oxigênio é mais eletronegativo do que o berílio e o enxofre, pois está mais à direita do que o primeiro e mais alto do que o enxofre.

Compare a afinidade eletrônica de dois elementos.
O Afinidade eletrônica é o mudança na energia que um átomo neutro sofre quando atrai um elétron para se tornar um íon negativo. Neste caso, a afinidade eletrônica não varia tão exatamente como nos casos anteriores, embora possamos dizer que, em geral, a afinidade eletrônica:
- Sobe, no mesmo período, da esquerda para a direita.
- Suba, no mesmo grupo, de baixo para cima.
Se você quiser ler mais artigos semelhantes a Para que serve a tabela periódica?, recomendamos que você insira nossa categoria de O átomo.
Referências
Você tem alguma opinião ou comentário sobre os usos da tabela periódica? Sinta-se à vontade para deixá-lo em nossa seção de comentários! Gostou deste artigo? Você também pode deixar sua classificação abaixo!