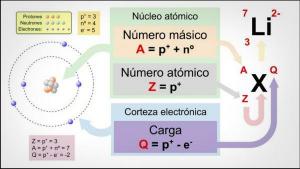
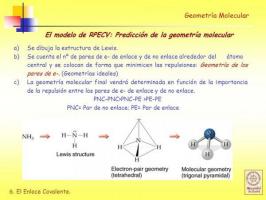
Geometria MOLECULAR: definição e exemplos
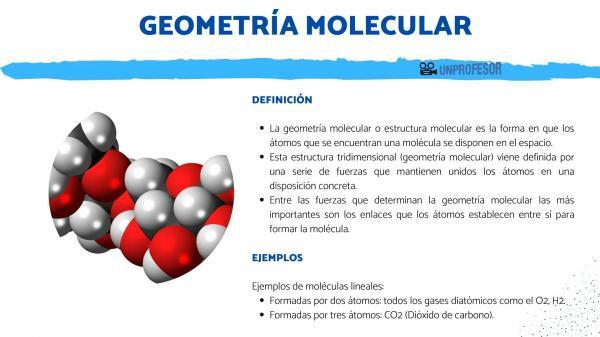
O forma tridimensional em que os átomos que compõem uma molécula são arranjados é conhecido pelo nome de geometria molecular ou estrutura molecular.
É possível deduzir a geometria dessas moléculas a partir de um modelo teórico: o modelo de repulsão dos pares de elétrons na camada de valência (RPECV). Este modelo é especialmente útil para representar a geometria de moléculas compostas de pequenos átomos e unidos por ligações covalentes (compartilhamento de elétrons).
Nesta lição de um PROFESSOR, descobriremos o definição de geometria molecular e exemplos Para que, desta forma, você possa aprender em que consiste o modelo RPECV, como a geometria das moléculas pode ser deduzida por este método e alguns exemplos.
Índice
- Definição de geometria molecular
- Exemplos de geometria molecular
- Conheça a estrutura de Lewis da molécula
- Modelo de repulsão de par de elétrons da camada de valência (RPECV)
Definição de geometria molecular.
Geometria molecular ou estrutura molecular é a maneira como os átomos encontrou uma molécula estão dispostos no espaço.
Esta estrutura tridimensional (geometria molecular) vem definido por uma série de forças que mantêm os átomos juntos em um arranjo específico. Entre as forças que determinam a geometria molecular, as mais importantes são os links que os átomos deitar um para o outro para formar a molécula.
A geometria das moléculas é muito importante porque determina quais são as características físico-químicas da matéria. Por exemplo: as moléculas de H2O têm uma geometria angular que é dada pelas ligações que as formam. A adoção dessa geometria angular torna a molécula de água um dipolo elétrico e tem propriedades excepcionais. Graças à sua geometria, a água é líquida à temperatura ambiente, é capaz de dissolver muitas substâncias, etc.
Obviamente, dado o tamanho das moléculas, sua geometria não pode ser observada diretamente e deve ser deduzida por métodos indiretos. Além disso, é necessário representar essas geometrias por meio de modelos teóricos.
São esses modelos teóricos que nos permitem determinar como é a geometria de uma molécula a partir de sua fórmula molecular.
Exemplos de geometria molecular.
Como vimos na seção anterior, os átomos que constituem uma molécula podem adquirir diferentes arranjos espaciais (geometrias). Nesta seção, veremos alguns exemplos de geometria molecular.
Geometrias bidimensionais
Em alguns casos, as moléculas adquirem geometrias planas ou bidimensionais, ou seja, são estruturas que possuem apenas duas dimensões e ocupam uma superfície (não possuem volume).
Geometria linear
É a geometria mais simples, trata-se de moléculas cujos átomos se unem para formar uma linha reta. Todas as moléculas compostas por dois átomos são lineares, mas essa geometria também ocorre em moléculas compostas por três átomos.
Exemplos de moléculas lineares:
Formado por dois átomos: todos os gases diatômicos, como O2, H2.
Composto por três átomos: CO2 (dióxido de carbono).
Geometria angular
Eles são moléculas compostas de três átomos que se juntam em um ângulo. A amplitude do ângulo formado pode ser diferente, dependendo do tipo de átomos que o formam. As amplitudes dos ângulos formados pelas moléculas angulares têm valores entre 90º e 120º.
Exemplos: H2O, SO2 (dióxido de enxofre), SnCl2 (dicloreto de estanho)
Geometria triangular
São moléculas compostas por quatro átomos, com um átomo localizado no centro de um triângulo imaginário e os outros três átomos restantes localizados em cada um dos vértices desse triângulo.
Exemplos: SO3 (trióxido de enxofre), NO3- (íon nitrato)
Geometria quadrada
Moléculas com esta geometria têm 5 átomos. Um está localizado no centro de um quadrado e o outro 4 em cada um dos vértices da figura.
Exemplos: XeF4 (trifluoreto de xenônio)
Geometrias tridimensionais
Eles têm três dimensões, ou seja, eles têm volume. As geometrias das moléculas 3D são muito diversas, aqui veremos apenas alguns exemplos.
Geometria tetraédrica
Esta geometria é aquela apresentada por algumas moléculas formadas por cinco átomos, nela um átomo está localizado em o centro de um cubo imaginário e os quatro átomos restantes estão localizados nos vértices do cubo (tetraedro).
Exemplo: CH4 (metano), MnO4-(íon permanganato)
Geometria piramidal trigonal
São moléculas com quatro átomos dispostos nos quatro vértices de uma pirâmide de base triangular.
Exemplo: NH3 (amônia), PH3 (fosfina)
Geometria piramidal quadrangular
Neste caso, o número de átomos que compõem a molécula é seis e cinco deles estão dispostos no vértices de uma pirâmide de base quadrada, enquanto o sexto ocupa o centro do quadrado do base.
Exemplo: ClF5 (pentafluoreto de cloro)
Conheça a estrutura de Lewis da molécula.
Antes que você possa usar o Método RPECV é preciso saber o que é Estrutura de Lewis da molécula e para isso você deve primeiro saber o que o configuração eletronicada camada de Valência dos diferentes átomos que compõem a molécula.
Portanto, antes de poder determinar a geometria de uma molécula é necessário realizar algumas etapas anteriores:
- PARA. Obtenha as configurações de elétrons dos diferentes átomos que compõem a molécula.
- B. Determine o número de elétrons da camada de valência de cada um dos átomos. Os elétrons na camada de valência são os elétrons que o átomo pode usar para formar ligações.
- C. Deduza a estrutura de Lewis levando em consideração quantos elétrons cada átomo possui em sua camada de valência.
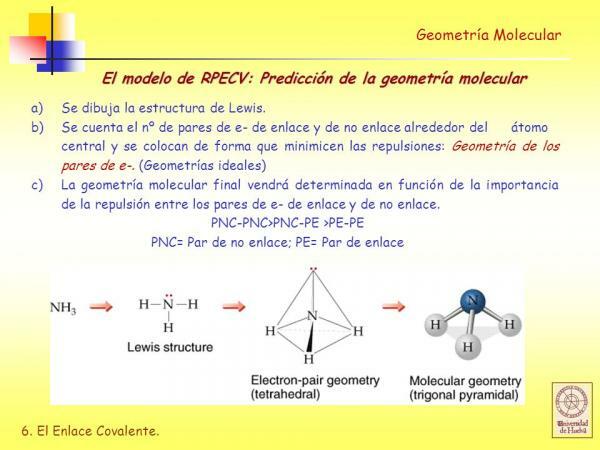
Imagem: Slideplayer
Modelo de repulsão de par de elétrons da camada de valência (RPECV)
Nas Estruturas de Lewis cada um dos átomos ligados, deve atender ao regra do octeto. Quando um átomo cumpre a regra do octeto, ele é cercado por quatro pares de elétrons que podem ser elétrons que fazem parte de um ligação (pares de elétrons de ligação) ou pares de elétrons que não participam da formação de ligações (pares de elétrons não obrigatório).
Como veremos, uma vez que a estrutura de Lewis de uma molécula é determinada, deduza sua geometria usando o modelo de repulsão dos pares de elétrons da camada de valência é muito fácil.
De acordo com esse modelo de representação, os ligantes (X) e os pares de elétrons não vinculantes (E) são dispostos em torno do átomo central (A), de forma que a distância entre eles seja máxima. A soma de ligantes e pares de elétrons não ligados (X + E) determina o tipo de geometria da molécula.
X + E = 2
Geometria Linear
AX2: Molécula formada por dois átomos ligantes ligados a um átomo central
Exemplo: hidreto de berílio (BeH2).
X + E = 3
Geometria do plano triangular (triângulo equilátero)
AX3: Molécula composta por três átomos ligados a um átomo central
Exemplos: Alguns cloretos, como boro ou alumínio (BCl3, AlCl3)
Geometria angular (ângulo de 120º)
AX2E: Molécula com um átomo central ligado a dois ligantes e um par de elétrons não ligado.
Exemplos: cloreto de estanho (II) (Sn2Cl)
X + E = 4
Geometria tetraédrica
AX4: Moléculas com um átomo central com quatro ligantes dispostos em ligações para que os ligantes sejam eles têm nos vértices das diagonais opostas um cubo cujo centro é o próprio átomo central.
Exemplos: Moléculas como metano (CH4), cloreto de silício (SiCl4) ou tetracloreto de carbono (CCl4) apresentam esta geometria.
Geometria da Pirâmide Trigonal
AX3E: Moléculas com 3 ligantes e 1 par de elétrons solitário em que os átomos dos três ligantes estão dispostos para formar a base de uma pirâmide com uma base triangular em que o átomo central está no vértice superior do referido pirâmide
Exemplos: uma das moléculas que possui essa geometria é a amônia (NH3).
Geometria angular (ângulo de 109º)
AX2E2: Os dois ligantes e o átomo central estão dispostos formando um ângulo de 109º
Exemplos: Água (H2O) é uma das moléculas que possuem esta geometria.
Geometria linear
AX3: Como há apenas um ligante ligado ao átomo central, a geometria é linear.
Exemplo: Fluoreto de hidrogênio ou ácido fluorídrico (HF).
X + E = 5
Geometria trigonal bipiramidal
AX5: A molécula tem a geometria de duas pirâmides opostas, com base triangular comum a ambas. O átomo central está organizado no centro e os ligantes estão localizados nos vértices.
Exemplo: pentacloreto de fósforo (PCl5)
Geometria dishenoidal
AX4E: Nesse tipo de geometria, os átomos adquirem um arranjo que lembra a estrutura de uma gangorra.
Exemplo: fluoreto de tetra enxofre (SF4).
Geometria T
AX3E2: As moléculas têm o formato da letra T, com os ligantes nas extremidades da letra e o átomo central no ponto onde as duas linhas que o formam se encontram.
Exemplo: trifluoreto de cloro (ClF3)
Geometria linear
AX2E3: Neste caso, os três átomos da molécula estão dispostos em linha com o átomo central em uma posição intermediária.
Exemplo: difluoreto de xenônio (F2Xe)
X + E = 6
Geometria octaédrica
AX6: Esse tipo de molécula tem uma estrutura que lembra um octaedro em que o átomo central ocuparia o centro da figura geométrica e os seis ligantes de cada um de seus vértices.
Exemplo: hexafluoreto de enxofre (SF6)
Pirâmide de base quadrada
AX5E: Nesse caso, os átomos formam uma figura em que o átomo central ocupa o centro da base e os ligantes os cinco vértices da figura.
Exemplo: pentafluoreto de bromo (BrF5)
Geometria quadrada plana
AX4E2: Os átomos adquirem um arranjo em forma de quadrado, no qual o átomo central ocupa o centro da figura e os ligantes cada um de seus vértices.
Exemplo: íon tetrafluoreto de xenônio (XeF4)

Se você quiser ler mais artigos semelhantes a Geometria molecular: definição e exemplos, recomendamos que você insira nossa categoria de O átomo.
Bibliografia
Alejandrina Gallego Picó, Rosa Mª Garcinuño Martínez, Mª José Morcillo Ortega, Miguel Ángel Vázquez Segura. (2018) Química básica. Madrid: Uned