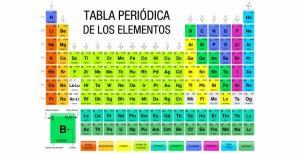
Na čo slúži PERIODICKÁ TABUĽKA?
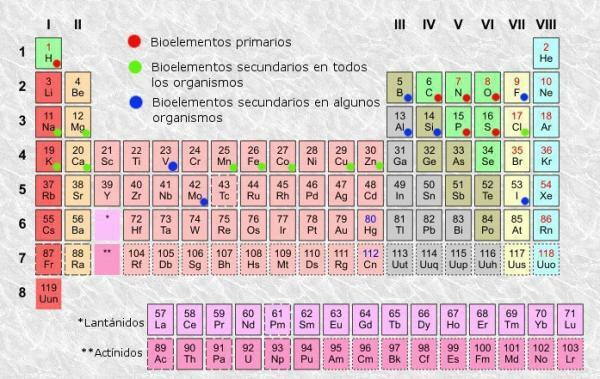
Periodická tabuľka je klasifikačný systém pre atómové prvky, ktorý vynašiel v roku 1869 ruský chemik Dmitrija Mendelejeva a neskôr ho reorganizovali a aktualizovali ďalší chemici, až kým sa nedostavil do svojho vzhľadu prúd. Napriek tomu, že ide o nástroj, ktorý sa v priebehu histórie osvedčil (preto sa naďalej používa a aktualizuje), jedná sa o také zdĺhavé učiť sa a rozumieť, a preto sme si všetci položili otázku „Na čo slúži tabuľka? periodicky? “.
Ak to chcete vedieť na čo slúži periodická tabuľka a prečo je dôležité pochopiť jeho vlastnosti, pokračujte v čítaní tejto lekcie od UČITEĽA.
Register
- Klasifikácia periodickej tabuľky
- Nájdenie názvu alebo symbolu prvku v periodickej tabuľke
- Poznajte atómovú hmotnosť prvku
- Poznajte atómové číslo prvku
- Predpovedajte atómový polomer prvku
- Porovnajte ionizačnú energiu dvoch prvkov
- Nájdenie elektronegativity chemického prvku
- Porovnajte elektrónovú afinitu dvoch prvkov
Klasifikácia periodickej tabuľky.
Ako v každej tabuľke, aj v
periodická tabuľka Z prvkov môžeme rozlíšiť stĺpce (zvislé) a riadky (vodorovné). V periodickej tabuľke je 18 stĺpcov alebo skupín a 7 riadkov alebo období.Okrem toho budete môcť overiť, že sa zvyčajne v každom z polí v tabuľke zobrazujú aspoň tieto informácie:
- Symbol chemického prvku: skratky alebo značky, ktoré sa používajú na identifikáciu prvkov. Zvyčajne sa skladajú z jedného alebo dvoch písmen, z ktorých prvé je vždy veľké.
- Názov chemického prvku: názov chemického prvku, ktorý zodpovedá hornej skratke. Spravidla je pod symbolom.
- Atómové číslo: celkový počet protónov, ktoré má každý atóm tohto prvku. Spravidla sa zobrazuje v ľavom hornom rohu poľa s položkami (alebo v pravom hornom rohu úplnejších tabuliek).
- Atómová hmotnosť: hmotnosť atómu sa dá bežne považovať za celkovú hmotnosť protónov a neutrónov v jednom atóme. Je k dispozícii pod názvom prvku v najjednoduchších tabuľkách, aj keď v iných sa môže zobraziť v pravej hornej časti okna prvku.
Existujú periodické tabuľky, ktoré obsahujú ďalšie zložitejšie a konkrétnejšie informácie ako napr oxidačné stavy (užitočné napríklad pri príprave chemických zlúčenín), ionizačná energia, elektronegativita atď., ale základné periodické tabuľky zvyčajne poskytnite dostatok informácií a sú zvyčajne dostatočné pre priemerného používateľa, ktorý z neho môže zistiť informácie, ako sú tie, ktoré vám hovoríme nižšie.

Zistite pomocou periodickej tabuľky názov alebo symbol prvku.
Niekedy vieme symbol chemického prvku ale jeho meno nepoznáme. Inokedy poznáme názov chemického prvku, ale nie jeho skratka alebo symbol. V skutočnosti je veľmi ľahké, že sa vám to niekedy stalo v triede.
V týchto prípadoch môžeme použiť periodickú tabuľku bez potreby zložitosti tabuľky a rýchlo a presne vyhľadať chýbajúce údaje.
Poznajte atómovú hmotnosť prvku.
Niekedy poznáme chemický prvok, s ktorým máme do činenia, ale potrebujeme vedieť jeho atómová hmotnosť, teda koľko váži atóm tohto prvku.
Tieto informácie budú užitočné napríklad pri vykonávaní nasledujúcich úloh:
- Vypočítajte konkrétne množstvo látky.
- Analyzujte výsledky získané v rámci testov alebo experimentov.
- Vypočítajte percento hmotnosti.
- Pochopte presné molárne hmotnosti zložitých molekúl.
Poznajte atómové číslo prvku.
Atómové číslo je celkový počet protónov, ktoré má atóm prvku. V elektricky neutrálnom atóme inom ako katión (kladne nabitý, s jedným elektrónom nižším ako je jeho normálny stav) alebo anión (záporne nabitý, s jedným ďalším elektrónom ako je jeho normálny stav), počet protónov sa rovná počtu protónov elektróny.
Počet protónov je rozhodujúcim faktorom pri rozlišovaní jedného prvku od druhého, pretože počet elektrónov alebo neutrónov nemení typ prvku.

Predpovedajte atómový polomer prvku.
Atómový polomer je polovica vzdialenosti medzi stredom dvoch atómov toho istého prvku, ktoré sa navzájom takmer nedotýkajú. V takom prípade poznajte poloha chemického prvku na periodickej tabuľke Môže nám pomôcť zistiť jeho približný atómový polomer alebo v porovnaní s iným prvkom. Preto to musíme vedieť atómový polomer:
- Zvyšuje sa pri prechode z hornej do dolnej časti periodickej tabuľky.
- Klesá to, keď sa periodickou tabuľkou pohybujeme zľava doprava.
Týmto spôsobom je vápnik menší ako rubídium, ale väčší ako železo.
Naučiť sa viac o Aký je atómový polomer s touto ďalšou video lekciou od UČITEĽA.
Porovnajte ionizačnú energiu dvoch prvkov.
The ionizačná energia je energia potrebná na odstránenie elektrónu z atómu prvku. V tomto prípade, ak poznáme polohu dvoch prvkov v periodickej tabuľke, môžeme vedieť, ktorý prvok bude jednoduchšie „odstrániť“ elektrón. Budeme musieť brať do úvahy iba to, že:
- Ionizačná energia klesá, keď sa pohybuje v periodickej tabuľke hore a dole.
- Ionizačná energia sa zvyšuje pri pohybe zľava doprava od periodickej tabuľky.
Medzi berýliom a kyslíkom má kyslík viac ionizačnej energie. Ak porovnáme kyslík a síru, ktoré sú v rovnakej skupine, ale v nasledujúcom období, má kyslík tiež vyššiu ionizačnú energiu, pretože je vyššia v periodickej tabuľke.
Nájdite elektronegativitu chemického prvku.
Elektronegativita je schopnosť atómu priťahovať elektróny. V praxi to znamená schopnosť vytvárať chemickú väzbu. Aby sme vedeli, či chemický prvok bude mať veľkú schopnosť vytvárať chemickú väzbu alebo nie, musíme brať do úvahy iba vzorec, ktorý nasleduje v periodickej tabuľke, to znamená:
- Pri pohybe hore a dole klesá.
- Zvyšuje sa pri pohybe zľava doprava.
Rovnako ako v predchádzajúcom prípade je kyslík elektronegatívnejší ako berýlium a síra, pretože je ďalej vpravo ako prvý a vyšší ako síra.

Porovnajte elektrónovú afinitu dvoch prvkov.
The Elektronická afinita je on zmena energie, ktorú podstúpi neutrálny atóm, keď priťahuje elektrón aby sa stal negatívnym iónom. V tomto prípade sa elektronická afinita nelíši tak presne ako v predchádzajúcich prípadoch, aj keď môžeme povedať, že všeobecne platí, že elektronická afinita:
- Stúpa v rovnakom období zľava doprava.
- Stúpajte v rovnakej skupine zdola nahor.
Ak si chcete prečítať viac podobných článkov Na čo slúži periodická tabuľka?, odporúčame vám vstúpiť do našej kategórie Atóm.
Referencie
Máte nejaké pripomienky alebo pripomienky k použitiu periodickej tabuľky? Pokojne to nechajte v našej sekcii komentárov! Páčil sa vám tento článok? Svoje hodnotenie môžete zanechať aj nižšie!