Čo sú CHEMICKÉ VZORCE a na čo slúžia [SÚHRN + VIDEÁ]
Aj keď sa to nezdá, chemické prvky periodickej tabuľky Obklopujú nás zo všetkých strán. Mnohokrát sa však nenachádzajú oddelene, ale tvoria molekuly alebo makromolekuly rôznych chemických prvkov. Chemické vzorce sú grafickým vyjadrením týchto zlúčenín a používajú sa na štandardizáciu ich nomenklatúry. V tejto lekcii od UČITEĽA uvidíme čo sú chemické vzorce a na čo slúžia. Pridajte sa k nám a dozviete sa viac!
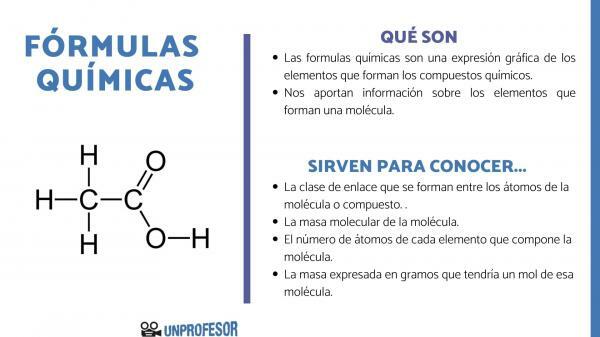
The chemické vzorce sú grafickým vyjadrením prvkov, ktoré tvoria chemické zlúčeniny.
Tieto chemické vzorce nie sú ľubovoľné, ale dodržiavajú niektoré prísne pravidlá chemickej nomenklatúry, ustanovenej IUPAC (Medzinárodná únia čistej a aplikovanej chémie).
Chemické vzorce nám tiež poskytujú informácie o prvky, ktoré tvoria molekulu, teda napríklad nám hovorí o počte a príslušných pomeroch každého z atómov, ktoré ho tvoria, a niekedy dokonca aj o type Chemická väzba ktorý existuje medzi týmito prvkami.
Každá molekula alebo makromolekula, ktorá existuje, zodpovedá svojmu chemickému vzorcu, nech už existujú
rôzne typy vzorcov. Každý z týchto typov nám poskytuje rôzne informácie o molekule, ale všetky nám pomáhajú jej porozumieť chemickej povahy a pomáha nám pochopiť, čo sa deje pri chemických reakciách a ako sa jedna zlúčenina môže premeniť na inú.Aby sme však porozumeli tejto chemickej nomenklatúre, je potrebné mať určité znalosti v chémii, pretože sa riadi pomerne špecializovaným technickým jazykom.

Obrázok: Slideplayer
The chemické vzorce sú zastúpené spojenie chemických symbolov, so zodpovedajúcim písmenom každého atómu, ako sa nachádza v periodická tabuľkaa dolné indexy, čo sú čísla, ktoré predstavujú ich množstvo atómov v molekule
V chémii (organickej aj anorganickej) existujú určité fragmenty alebo zlúčeniny, ktoré vykazujú určitú recidívu štrukturálnu aj funkčnú a sú identifikované menami špecifické. Keď tieto fragmenty majú voľné elektróny, ktoré nie sú zdieľané, nazývajú sa radikálmi a sú to nestabilné, vysoko reaktívne zlúčeniny s krátkym polčasom rozpadu.
Príkladmi radikálov sú metylové skupiny CH3, dusičnanové skupiny NO3hydroxylové skupiny OH- alebo radikál Cl-. Sú však známe ako funkčné skupiny, keď sú atómami alebo skupinami atómov pripojených k reťazcu oxidu uhličitého (s rôznym uhlíkom) a ktoré sú zodpovedné za reaktivitu a chemické vlastnosti molekuly.
Tieto skupiny sú obzvlášť dôležité v organickej chémii (ľudské biomolekuly sú v podstate uhlík a vodík). Niekoľko príkladov funkčných skupín sú karbonylová skupina = C = O alebo karboxylová skupina -COOH.

Obrázok: Monogramas.com
Ako sme povedali, existuje niekoľko typov chemických vzorcov. Každý z týchto vzorcov nám poskytuje iný typ informácií o molekulách, a preto slúži konkrétnemu cieľu bez toho, aby bol nejaký vzorec vo všeobecnosti lepší alebo horší ako iný.
Triedy chemických vzorcov, ktoré rozlišujeme, sú:
Empirické vzorce
Empirické vzorce sú najjednoduchšie vzorce reprezentujúce chemickú molekulu, niekedy sa hovorí, že ide o minimálne vzorce. Tieto vzorce predstavujú podiel atómov každého z prvkov v molekule, ktoré sú zjednodušené na celé čísla, vždy najmenšie. Príkladom tohto vzorca je CH3 (metylová skupina) s tromi atómami vodíka a jedným atómom uhlíka.
Tieto vzorce však môžu niekedy poskytnúť mylné predstavy o zložení molekuly. K tomu dochádza, keď vzorec neudáva skutočný počet atómov v molekule, ako pri peroxide vodík, ktorého empirický vzorec je HO, pričom vzorec by mal byť H2O2 (dva atómy vodíka a dva kyslík). Deje sa tak prostredníctvom nomenklatúrnej konvencie, keďže oba indexy sú rovnaké, sú zjednodušené.
Niektoré zlúčeniny však môžu byť reprezentované iba empirickými vzorcami, pretože sú tvorené iónovými sieťami. K tomu dochádza napríklad v kuchynskej soli alebo chloride sodnom, ktorý je reprezentovaný ako NaCl, čo znamená, že každý sodík obsahuje chlór.
Molekulárne vzorce
Tieto typy vzorcov sú celkom základné, jednoducho vyjadrujú typ atómov a počet každého z nich prítomných v kovalentnej molekule. Sú to vzorce, ktoré prezentujú chemické prvky a číslo lineárnym spôsobom (vo forme dolného indexu. Príkladom tohto typu vzorca je, keď sa glukóza nazýva C6H12O6, čo vyjadruje túto glukózu Molekula glukózy sa skladá zo šiestich atómov uhlíka, dvanástich atómov vodíka a šiestich kyslík.
Molekulové vzorce sú široko používané, niekedy hovoria, že sú to skutočné vzorce molekúl. V mnohých prípadoch sa zhodujú s empirickými vzorcami, napríklad v CO2.
Polorozvinuté vzorce
Polorozvinuté vzorce sú typom vzorcov podobných molekulovým vzorcom, pretože tiež vyjadrujú atómy, ktoré tvoria molekulu a ich počet, ale aj poskytnúť informácie o chemických väzbách (reprezentovaných čiarami medzi atómami) a type väzby medzi atómami uhlíka, ktoré ju tvoria (ak sú jednoduché, dvojité resp. trojičky). Polorozvinutý vzorec je užitočný na identifikáciu radikálov, ktoré tvoria molekulu a jej chemickú štruktúru (nie sú znázornené väzby medzi atómami uhlíka a vodíka).
V prípade glukózy je jej polorozvinutý vzorec CH2OH - CHOH - CHOH - CHOH -CHOH - CHO a ako vidno atómy uhlíka, vodíka a kyslík sú rovnaké ako v molekulovom vzorci (šesť, dvanásť a šesť) a všetky jednoduché väzby (glukóza má iba väzby jednoduché). Tento vzorec je preto zložitejší ako vzorec molekulový.
Polorozvinuté vzorce sa niekedy nazývajú kondenzované a sú možno najpoužívanejšou triedou vzorcov. používané najmä v organickej chémii, aj keď nám neumožňujú pozorovať skutočnú geometriu molekúl.
Vyvinutý vzorec
Vyvinuté vzorce sú o niečo zložitejšie ako polorozvinuté. V tomto type vzorcov sú väzba a umiestnenie každého atómu v molekule znázornené v karteziánskej rovine, kým nie je znázornená celá zlúčenina.
Štrukturálny vzorec
Štrukturálny vzorec je grafické znázornenie štruktúry molekuly v priestore, ktoré nám poskytuje informácie o poradí a rozložení atómov v priestore. V tomto vzorci sú tiež znázornené chemické väzby, ktoré tvoria molekulu a či sú jednoduché, dvojité alebo trojité. Tento vzorec je teda tým, ktorý nám poskytuje najviac informácií o molekule.
Tieto typy vzorcov sa viac používajú na profesionálnej úrovni vo svete chémie, pretože umožňujú oveľa jasnejšie vidieť chemické reakcie alebo syntézu nových molekúl.
Lewisove vzorce
Ide o zložité, veľmi špecifické a technické vzorce. Sú tiež známe ako Lewisove diagramy alebo štruktúry a sú podobné vyvinutým vzorcom molekúl, ale Okrem toho sú označené elektróny, ktoré atómy zdieľajú v každej chemickej väzbe, ktoré sa líšia v závislosti od mocnosti atómov zapojené.
V týchto vzorcoch sú väzby medzi atómami znázornené čiarami (tiež označujúcimi, či sú jednoduché, dvojité alebo trojité) alebo s párom bodiek. Osamotené elektróny alebo elektróny, ktoré nie sú zdieľané vo väzbe, sú reprezentované bodmi okolo atómu, ktorému zodpovedá.

Obrázok: Organická chémia
Pri písaní vzorcov sa niekedy odkazuje naoxidačné číslo prvku (je častý v iónových zlúčeninách). Ide o súbor kladných a záporných čísel, ktoré idú spojené s každým prvkom.
- Oxidačné čísla možno interpretovať ako počet elektrónov že prvok sa podieľa na kovalentnej väzbe alebo sa prenáša v iónovej väzbe.
- Keď oxidačné znamienko nad atómom je negatívne, znamená, že tento prvok zachytáva elektróny a číslo, ktoré ho sprevádza vedľa neho, je počet zachytených elektrónov. Preto oxidačný stav -1 znamená, že prvok zachytí jeden elektrón, -2, ktorý zachytí dva atď.
- Keď je znak oxidácie pozitívne, atóm sa vzdá elektrónu a číslo, ktoré sprevádza tento znak, je počet odovzdaných elektrónov. Podobne oxidačný stav +1 znamená, že poskytuje jeden elektrón, +2, že poskytuje dva, atď.
Toto funguje väčšinou pre iónové zlúčeniny, v kovalentných väzbách, aj keď je interpretácia podobná, nie je rovnaká, pretože tieto väzby zdieľajú elektróny. V týchto zlúčeninách hovoríme o elektronegatívnych prvkoch, ktoré ťahajú väčšiu časť elektrónového páru a zostáva im zápornejší náboj v závislosti od počtu elektrónov, ktoré priťahujú. Toto je možné vidieť v Lewisove vzorce.
Ak chcete vedieť, na čo slúžia chemické vzorce, musíte vziať do úvahy, že toto číslo nám umožňuje nejaké získať informácie o molekule, ako sú:
- The trieda odkazov ktoré sa tvoria medzi atómami molekuly alebo zlúčeniny. Tieto väzby sú normálne kovalentné, ak sa na nich zúčastňujú nekovové a iónové atómy, ak ide o kovové a nekovové väzby.
- The molekulová hmotnosť molekuly.
- The počet atómov každého prvku, ktorý tvorí molekulu. Niekedy sa nazýva centezimálne zloženie molekuly.
- Hmotnosť vyjadrená v gramov ktorý by mal jeden mol tejto molekuly.
V prípade iónovej zlúčeniny, napríklad chloridu sodného alebo kuchynskej soli, to nie je úplne správne hovoriť o molekulách (aj keď sa to niekedy robí), že tieto majú tendenciu vytvárať veľké agregáty a makromolekuly. V tomto prípade nám vzorec zlúčeniny pomáha zistiť, ktoré ióny ju tvoria a v akom množstve.



