De 10 typerna av kemiska grundämnen (förklarade och klassificerade)
Hur många kemiska grundämnen måste finnas i universum? Denna fråga har fortfarande en lång väg att gå, eftersom forskare då och då skapar sina egna konstgjorda kemiska element.
Vad vi dock kan svara på är hur många typer av kemiska grundämnen måste finnas, något som vi får reda på härnäst.
- Relaterad artikel: "De 11 typerna av kemiska reaktioner"
Typerna av kemiska grundämnen
I naturen kan vi hitta alla slags ämnen. Dessa ämnen finns vanligtvis inte i rent tillstånd, utan är resultatet av kombinationen av olika element eller material som genom olika reaktioner, processer och tidsperioder har gett upphov till alla slags materia. Det finns inget i universum som inte är resultatet av kombinationen av atomer som tillhör olika typer av kemiska grundämnen, som vi kommer att se på djupet.
Men innan vi tittar på typerna av kemiska grundämnen, låt oss göra en liten genomgång av gymnasiet och komma ihåg vad kemiska element är.
Vi kallar "kemiskt element" materia som består av samma typ av atom, det vill säga ett ämne som är atomiskt rent.
Kemiska element kan inte sönderdelas till enklare och klassificeras i det periodiska systemet av elementen som rena material i universum.Men akta dig! Vi får inte blanda ihop element med enkla ämnen, eftersom två eller flera atomer av samma grundämne kan komponera i vissa fall molekyler grupperade på olika sätt som gör att några av de fysiska egenskaperna hos elementet i fråga varierar, dessa fall är isotoper. Till exempel är diamant och kol ämnen gjorda av det kemiska elementet kol (C). men det är organiserat på olika sätt och resulterar i två helt olika material.
Carl sagan Det stod att vi är stjärnstoft som reflekterar över stjärnor. Denna vackra fras är inte bara en metafor, utan ett vetenskapligt faktum. Kemiska element bildas, så vitt vi vet, inuti stjärnor som är resultatet av komplex fusions- och atomklyvningsprocesser som genererar allt tyngre element, resultatet av en process som kallas nukleosyntes.
De flesta av de kända elementen kan erhållas från naturen, hittas spontant eller bildar föreningar med andra element som uran (U), kol (C), kisel (Si), silver (Ag) eller guld (Au). Andra har å andra sidan tillverkats i laboratorier som americium (Am), berkelium (Bk) eller curium (Cm). Oavsett dess metod för att erhålla det eller om det finns i naturen, beroende på dess egenskaper, kommer det kemiska elementet i fråga att ha vissa användningsområden eller andra.
För närvarande är cirka 118 kemiska grundämnen kända, men med tanke på att människor har kunnat tillverka nya grundämnen är det en tidsfråga innan det periodiska systemet expanderar.
- Du kanske är intresserad av: "De två typerna av el (förklarad)"
Huvudtyperna av kemiska grundämnen
De viktigaste typerna av kemiska grundämnen är representerade i det periodiska systemet, ett system av klassificering skapad av den ryska kemisten Dmitri Mendeleev (1834-1907) som lade grunden 1869. Kemiska element ordnas visuellt baserat på deras egenskaper och egenskaper.
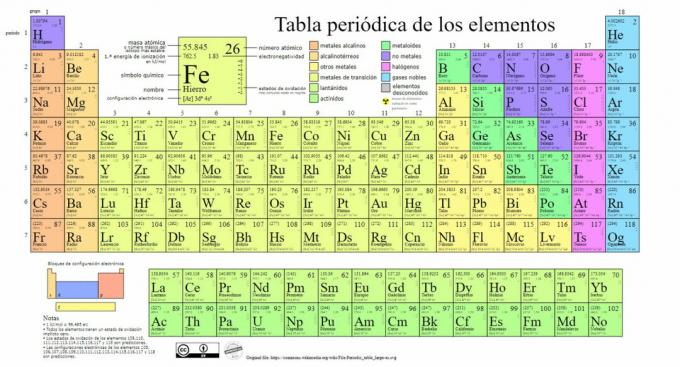
Med tiden och eftersom kemi gjorde viktiga vetenskapliga upptäckter skulle denna tabell utvidgas i följd, nå den form den har idag med de 118 element som hittills är kända.
För närvarande kan vi i denna tabell hitta följande typer av kemiska grundämnen:
1. Metaller
Metaller är kemiska grundämnen som i allmänhet innehåller mellan en och tre elektroner i atomens sista omlopp, elektroner som enkelt kan överföras gör dem till ledare av värme och elektricitet.
Metaller är vanligtvis formbara och segbara, med en karakteristisk glans vars intensitet beror på rörelsen hos elektronerna som utgör deras atomer. För det mesta är metaller fasta vid rumstemperatur, förutom kvicksilver.
Bland metaller hittar vi guld (Au), silver (Ag), koppar (Cu) och aluminium (Al) vars fysiska egenskaper gör dem till magnifika ledare av elektricitet, även om deras närvaro i naturen är mycket varierad, återspeglas i skillnaden mellan deras vikter.
Man tror att 75% av de kemiska grundämnen som finns i naturen är metaller, medan de återstående 25% består av ädelgaser, metalloider och andra typer.
Det finns klassificeringar inom denna kategori, som hittar aktinider, lantanider, övergångsmetaller, alkalimetaller, jordalkalimetaller och andra metaller.
- Relaterad artikel: "10 livsmedel med hög zinkhalt"
1.1. Lantanider
Lantanidelement finns i avlagringar som består av många mineraler. De är vita metaller som lätt oxiderar när de kommer i kontakt med luft. Bland dem hittar vi Lanthanum (La), Promethium (Pm), Europium (Eu) och Ytterbium (Yb).

- Du kanske är intresserad av: "De fem typerna av kemiska bindningar: så här består materia"
1.2. Actinides
Alla isotoper av aktinider är radioaktiva. Bland dem hittar vi actinium (Ac), uran (U), plutonium (Pu) och einsteinium (Es).
1.3. Övergångsmetaller
Övergångsmetaller finns i den centrala delen av det periodiska systemet. Dess främsta egenskap är att har elektronisk konfiguration av "d" -banan delvis fylld med elektroner.
I denna grupp finns det ämnen av alla slag och enligt dess bredaste klassificering skulle det motsvara kemiska element från 21 till 30, från 39 till 48, från 71 till 80 och från 103 till 112, totalt fyrtio och bland dem skulle vi hitta vanadin (V), rutenium (Ru), silver (Ag), tantal (Ta) och lawrencio (Lr).

1.4. Alkaliska metaller
Alkalimetallerna är en grupp av sex grundämnen som består av litium (Li), natrium (Na), kalium (K), rubidium (Rb), cesium (Cs) och francium (Fr). De är glänsande, mjuka metaller, mycket reaktiva vid normal temperatur och tryck och tappar lätt sin yttre elektron, belägen i deras "s" orbital.
1.5. Alkaliska jordar
Jordalkalimetallerna är en grupp element där vi hittar beryllium (Be), magnesium (Mg), kalcium (Ca), strontium (Sr), barium (Ba) och radium (Ra). Dess namn kommer från namnet på dess oxider, "jordar", som har grundläggande eller alkaliska egenskaper.
Alkaliska jordar de är hårdare än alkaliska, lyser och är bra elektriska ledare. De är mindre reaktiva än alkaliska och fungerar som bra reduktionsmedel. De har förmågan att bilda joniska föreningar och de har alla två elektroner i sitt yttersta skal.

1.6. Andra metaller
Kategorin "andra metaller" är en typ av ämnen som finns här eftersom du inte riktigt vet var du ska placera dem.
De är metalliska element som finns i det periodiska systemet tillsammans med metalloiderna i p -blocket. De tenderar att vara mjuka med låga smältpunkter. Bland dem finns bland annat aluminium (Al), indium (In), tenn (Sn) och vismut (Bi).

2. Inga metaller
Icke -metaller har i allmänhet mellan fem och sju elektroner i sin sista bana, en egenskap som gör att de får elektroner istället för att ge upp dem och därmed lyckas de ha åtta elektroner som därmed stabiliserar dem som atomer.
Detta element de är mycket dåliga ledare för värme och elektricitet. Till detta har de inte en karakteristisk glans, är inte särskilt formbara, inte särskilt sega och är mycket sköra i fast tillstånd. De kan inte rullas eller töjas, till skillnad från metaller.
De är mestadels viktiga för biologiska system, eftersom de finns i organiska föreningar, såsom svavel (S), kol (C), syre (O), väte (H) och jod (I).

- Relaterad artikel: "De 20 typerna av ädelstenar (beskrivna och med bilder)"
3. Metalloider
Som namnet antyder är metalloider en mellanliggande klassificering mellan metaller och icke-metaller som har egenskaper hos båda grupperna. Detta beror på att de har fyra atomer i sin sista bana, en mellanliggande mängd till metaller och icke-metaller.
Dessa kemiska element leder elektricitet endast i en riktning, så att de inte kan utföras i motsatt riktning som i metaller. Ett exempel på detta finns i kisel (Si), en metalloid som används vid tillverkning av halvledarelement för elektronikindustrin tack vare denna egenskap.
Andra metalloider är: bor (B), arsenik (As), antimon (Sb) och polonium (Po).

4. Halogener
Halogener är en grupp med sex element som de tenderar att bilda molekyler som består av två atomer (diatomiska) mycket kemiskt aktiva på grund av deras elektronegativitet.
Dessa ämnen förekommer vanligtvis i form av joner, det vill säga elektriskt laddade molekyler, som i detta fall är mononegativa, starkt oxiderande. Detta innebär att halogener är frätande och frätande ämnen.
Halogenerna är: fluor (F), klor (Cl), brom (Br), jod (I), astat (At) och tenese (Ts).

5. ädelgaser
Ädelgaserna är en grupp på sju vars naturliga tillstånd är gasformigt. De förekommer vanligtvis i form av diatomiska molekyler med mycket låg reaktivitet, det vill säga att de inte reagerar med andra element som utgör andra ämnen och av samma anledning är de kända som inerta gaser. Detta beror på att i sin sista bana finns det maximala antalet elektroner som är möjliga för den nivån, totalt åtta.
Denna utvalda grupp av element består av helium (He), neon (Ne), argon (Ar), krypton (Kr), xenon (Xe), radon (Rn) och oganeson (Og), tidigare känt som ununoctium.



